 Il nucleo dell'atomo è costituito da un certo numero di protoni e da un certo numero di neutroni. Se più atomi della stessa materia si uniscono insieme, essi formano una molecola. Le molecole fondamentali per un essere vivente sono:
Il nucleo dell'atomo è costituito da un certo numero di protoni e da un certo numero di neutroni. Se più atomi della stessa materia si uniscono insieme, essi formano una molecola. Le molecole fondamentali per un essere vivente sono:
Proteine e mioglobina
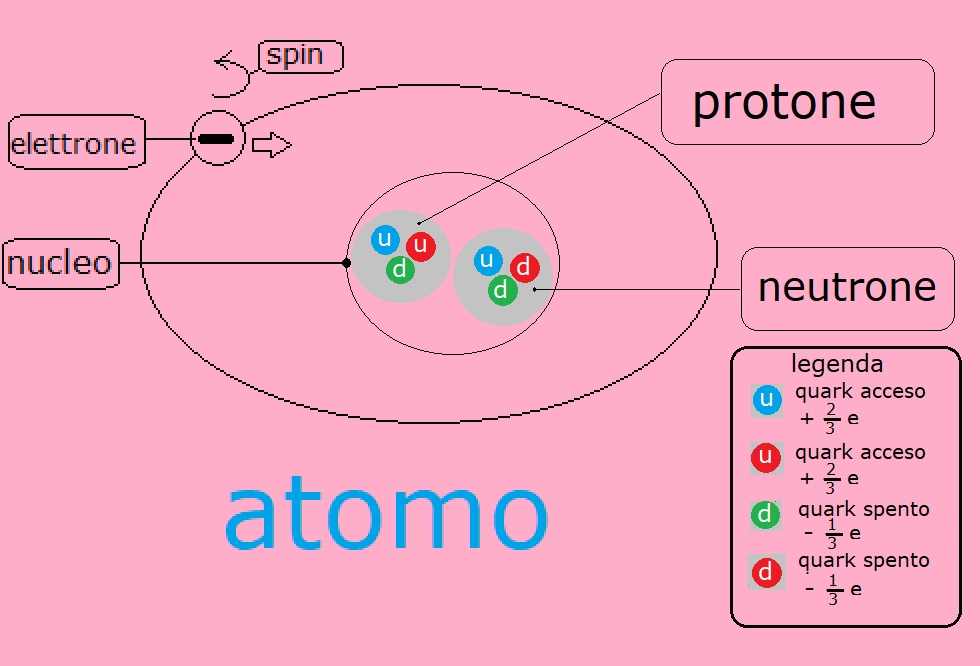
Riepilogo di argomenti precedentiLa parte più piccola, sia della materia vivente che della materia non vivente, viene chiamata atomo.
 Il nucleo dell'atomo è costituito da un certo numero di protoni e da un certo numero di neutroni. Se più atomi della stessa materia si uniscono insieme, essi formano una molecola. Le molecole fondamentali per un essere vivente sono:
Il nucleo dell'atomo è costituito da un certo numero di protoni e da un certo numero di neutroni. Se più atomi della stessa materia si uniscono insieme, essi formano una molecola. Le molecole fondamentali per un essere vivente sono:
L'idrogeno
L'idrogeno è un gas e si indica con la lettera maiuscola H. Quando due atomi si trovano vicini si attraggono a vicenda e si forma una molecola di idrogeno. Il simbolo H2 indica che una certa molecola ha due atomi di idrogeno.
L'ossigeno
Se ogni atomo ha 8 elettroni e 8 protoni forma un altro elemento detto ossigeno; l'ossigeno è un gas; ha numero atomico 8; si indica con la lettera O maiuscola. L'ossigeno si trova nell'aria che respiriamo, ma si trova anche nell'acqua.
L'acqua.
L'acqua è un composto chimico, formato da due atomi di idrogeno e da un atomo di ossigeno. La formula dell'acqua è: H2O
Il 2 usato come pedice, cioè messo sotto la lettera H, indica che gli atomi di idrogeno, cioè H, sono 2. La lettera O non ha un numero sotto, e quindi vuol dire che vi è un solo atomo di ossigeno. L'acqua è quindi composta da molecole e non è composta da un solo elemento, ma da due elementi, cioè idrogeno ed ossigeno. L'acqua è fondamentale per gli esseri viventi. Il nostro corpo è composto da circa il 65% di acqua.
Il carbonio
Se ogni atomo ha 6 elettroni e 6 protoni forma un altro elemento detto carbonio; il carbonio ha numero atomico 6; il carbonio si indica con la lettera C maiuscola; la grafite, cioè la parte interna di colore scuro che si trova nelle matite non colorate, è fatta di carbonio; cioè da molecole di carbonio molto tenere; infatti quando premiamo la matita su di un foglio di carta essa si deteriora, lasciando un solco di se stessa sulla carta. La grafite è un buon conduttore di corrente elettrica; la grafite si autolubrifica, cioè non ha bisogno di un liquido per scorrere; infatti deteriorandosi scorre dolcemente sul foglio di carta. Il carbonio è solido, cioè non è liquido come l'acqua, né un gas come l'ossigeno e l'idrogeno. Il carbonio puro non conduce la corrente elettrica; mentre l'acqua conduce molto bene la corrente elettrica; questo della corrente elettrica è fondamentale per la vita, cioè per gli esseri viventi e quindi per il nostro corpo. Infatti la corrente ha bisogno di due sostanze fondamentali, una che conduce la corrente e l'altra che fa da isolante, cioè una sostanza che non conduce la corrente, come la plastica che si trova sui fili che usiamo per caricare il telefonino. Il carbonio è alla base di tutti gli esseri viventi; un essere si dice vivente quando nasce, cresce, si riproduce, muore. La parte della chimica che studia il carbonio si chiama chimica organica. Il carbonio si unisce facilmente con gli altri elementi esistenti in natura. Una caratteristica del carbonio è quella di formare delle lunghe catene di atomi.
L'azoto
Se ogni atomo ha 7 elettroni e 7 protoni forma un altro elemento detto azoto; l'azoto ha numero atomico 7; l'azoto si indica con la lettera N maiuscola; l'azoto è un gas inerte e costituisce circa il 78% dell'aria che respiriamo.
Le proteine sono formate da lunghe catene di molecole; le molecole che compongono le proteine sono molto grandi come dimensioni, per cui sono dette macromolecole, cioè molecole grandi.

Con la lettera R indichiamo il gruppo laterale dell'amminoacido, cioè il gruppo R. Mediante il gruppo R si distinguono amminoacidi basici, amminoacidi acidi, amminoacidi idrofili, cioè che si legano con l'acqua, amminoacido idrofobi, cioè che non si legano con l'acqua.
La proteina nasce quando si uniscono i due componenti di essa; questo si ha nella crescita delle cellule che compongono il nostro corpo; quando, invece, mangiamo un cibo, la proteina del cibo si spezza nei due componenti che la costituiscono e quindi muore, diventando cibo per le cellule. La proteina non ha una vita molto lunga; alcune proteine durano alcuni minuti, altre proteine durano alcuni anni; nella cellula la proteina dura solo uno o due giorni. Ciascuno dei due componenti della proteina è detto amminoacido.
Formazione di una proteina

L'amminoacido si trova sotto forma di gas. Sottraendo calore a due amminoacidi posti nelle loro vicinanze si ha la condensazione, cioè si passa dalla forma gassosa alla forma liquida.

Un atomo di idrogeno, carico positivamente, H+ del secondo componente si stacca dall'atomo di azoto N e si unisce al gruppo OH+ del primo componente, formando una molecola di acqua, cioè H2O.
Il componente di sinistra, resta carico positivamente, avendo perso uno ione OH+; mentre il componente di destra resta carico negativamente, avendo perso uno ione H+. I due componenti della proteina si attraggono e restano uniti mediante un legame di tipo covalente. Questo legame è detto legame peptidico, cioè legame caratteristico della proteina. La proteina a due componenti si chiama dipeptide, cioè ha due componenti. Questa prima proteina ha essa stessa ai due estremi una parte acida a destra e un parte basica a sinistra; di conseguenza si può legare ad un altro componente amminoacido oppure ad un altra proteina costituita da due componenti. Si forma in tal modo una lunga catena a molti componenti; questa lunga catena si chiama polipeptide, cioè è costituita da molti componenti. Per chiamarsi proteina deve avere almeno 20 componenti amminoacidi. Togliendo l'acqua che si forma la reazione chimica avviene più velocemente. Il fenomeno è reversibile. Cioè se prendiamo una proteina già formata e aggiungiamo acqua, la proteina si scioglie, cioè ritorna nella sua forma iniziale; si hanno, cioè, i componenti di partenza. Questo fenomeno è detto idrolisi, cioè scioglimento dei legami peptidici usando acqua come solvente. La idrolisi è favorita dalla presenza di enzimi. L'enzima in biochimica è una proteina che velocizza le reazioni chimiche; l'enzima si comporta come un catalizzatore, cioè velocizza la reazione chimica. La idrolisi avviene per esempio nella digestione dei cibi.
Ci sono molte proteine nel corpo umano; difficile è elencarle tutte. Ricordiamo la mioglobina.
La mioglobina è una proteina che lega l'ossigeno del sangue. La mioglobina si trova nei muscoli dell'uomo e non nel sangue; per cui, se la si ritrova nel sangue, vuol dire che qualche muscolo si è rovinato, cioè si è lesionato. La mioglobina non va confusa con la emoglobina. La mioglobina lega una sola molecola di ossigeno alla volta. Il processo è reversibile. La mioglobina si trova nei muscoli ed ha un colore rosso.
La mioglobina è costituita da una sola catena composta da 153
amminoacidi; questa catena è avvolta su se stessa; gli enzimi si trovano insieme
alla mioglobina e non in un altro punto del corpo, come avviene per la
emoglobina.

Ogni singola catena di mioglobina contiene al suo interno una parte non proteica, detta eme. L'eme funziona da cofattore, cioè rende possibile e velocizza la reazione chimica, grazie alla presenza dello ione di ferro Fe2+. Quando la mioglobina si lega con l'ossigeno si chiama ossimioglobina, cioè mioglobina legata con ossigeno.

Legandosi con l'ossigeno lo ione del ferro diventa Fe3+ e il superossido di ossigeno che si forma si lega subito alla istidina, un amminoacido sempre presente nello stesso muscolo dove si trova la mioglobina.
Un'altra proteina e la emoglobina.
La emoglobina è una proteina che si trova nei globuli rossi del sangue; l'emoglobina lega l'ossigeno del sangue e lo trasporta, tramite il sangue, nelle cellule a cui è destinato. Quando il sangue arriva nei polmoni, l'ossigeno dell'aria inspirata si lega alla emoglobina. Quando poi l'emoglobina arriva, tramite il sangue, nelle cellule da ossigenare, l'ossigeno viene ceduto alle cellule del tessuto o organo da ossigenare.
Quando la emoglobina si lega con l'ossigeno si chiama ossiemoglobina, cioè emoglobina legata con ossigeno. Quando la emoglobina cede l'ossigeno si chiama deossiemoglobina, cioè emoglobina che ha ceduto ossigeno e quindi non contiene ossigeno da cedere.
Gli enzimi, che facilitano le reazioni chimiche, non si trovano insieme alla
emoglobina.

La emoglobina è costituita da 4 lunghe catene di amminoacidi. Ogni singola catena di emoglobina contiene al suo interno una parte non proteica, detta eme. L'eme funziona da cofattore, cioè rende possibile e velocizza la reazione chimica, grazie alla presenza dello ione di ferro Fe2+
Ogni molecola di emoglobina può legarsi al massimo a 4 molecole di ossigeno O2; si dice saturazione quando le molecole di ossigeno sono 4, cioè si ha il 100% di saturazione. Se, invece, lo molecole di ossigeno sono 2, cioè la metà del massimo, si ha saturazione al 50%. Quando l'emoglobina si trova nei polmoni essa si trova allo stato rilassato, detto Stato R, cioè è in grado di legarsi facilmente con l'ossigeno; quando la emoglobina giunge nelle cellule da ossigenare, essa si trova nello stato teso, detto Stato T; nello Stato T la emoglobina non si lega facilmente con l'ossigeno, ma tende a cederlo alle cellule.

Nei globuli rossi del sangue è presente anche il 2,3-bisfosfoglicerato, con una concentrazione uguale a quella della emoglobina. Il 2,3-bisfosfoglicerato riduce la proprietà della emoglobina di legarsi con l'ossigeno. La concentrazione di 2,3-bisfosfoglicerato dipende dalla pressione atmosferica esterna in cui ci troviamo in un certo momento. La pressione atmosferica è alta se ci troviamo a livello del mare; la pressione atmosferica è bassa se ci troviamo in montagna. Per cui se andiamo in auto dal mare in montagna la pressione atmosferica si riduce e meno ossigeno viene fornito dai polmoni alla emoglobina; per cui meno ossigeno si trova nei tessuti. Nei primi giorni la percentuale di 2,3-bisfosfoglicerato nei globuli rossi è bassa; quindi la emoglobina trattiene per se l'ossigeno e non lo rilascia nei tessuti. Man mano che la percentuale di 2,3-bisfosfoglicerato aumenta nei globuli rossi, la emoglobina riduce la sua affinità con l'ossigeno e lo cede più facilmente ai tessuti.